۱. متانول: خواص، کاربردها
در این پست به بررسی ترکیب شیمیایی متانول می پردازیم. اهمیت این ترکیب همه کاره، خواص منحصر به فرد و طیف گسترده ای از کاربردهای آن در صنایع مختلف را کشف کنید. در این بررسی تاثیر متانول بر زندگی و محیط زیست ما به ما بپیوندید.
۲. نام شیمیایی و پیشینه:
۲.۱ نام شیمیایی کامل:
متانول که به نام متیل الکل یا الکل چوب نیز شناخته می شود، مایعی بی رنگ و فرار با فرمول شیمیایی CH3OH است. این ساده ترین الکل است که از یک گروه متیل (-CH3) متصل به یک گروه هیدروکسیل (-OH) تشکیل شده است.
۲.۲ نام های جایگزین:
متانول معمولاً به عنوان الکل متیل، الکل چوب یا کاربینول شناخته می شود.
۲.۳ سابقه تاریخی:
متانول برای قرن ها توسط انسان استفاده می شده است. حضور آن در منابع طبیعی، مانند نوشیدنی های تخمیر شده، در اوایل تشخیص داده شد. با این حال، شناسایی علمی و تولید آن در مقادیر قابل توجهی از قرن ۱۹ آغاز شد. در سال ۱۶۶۱، رابرت بویل تقطیر مخرب چوب را توصیف کرد که بخار قابل اشتعال تولید کرد که بعداً به عنوان متانول شناخته شد. در اواخر قرن نوزدهم، تولید تجاری متانول توسط فردریش آگوست فون استرادونیتز تأسیس شد.
۲.۴ حقایق جالب:
• متانول یک ترکیب بسیار متنوع با کاربردهای متعدد، از مصارف صنعتی گرفته تا تولید انرژی است.
• معمولاً از طریق سنتز مونوکسید کربن و گاز هیدروژن، فرآیندی که به عنوان سنتز متانول شناخته می شود، تولید می شود.
• متانول نسبت به باتری های سنتی چگالی انرژی بالاتری دارد و می تواند به عنوان سوخت جایگزین در پیل های سوختی یا به عنوان افزودنی بنزین استفاده شود.
• این ماده سمی است و باید با احتیاط رفتار کرد. مصرف متانول می تواند اثرات شدید سلامتی، از جمله نابینایی و یا حتی مرگ ایجاد کند.
۳. ساختار شیمیایی:
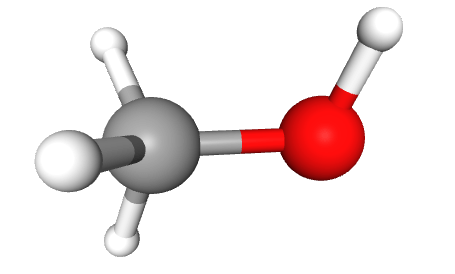
تصویر سه بعدی مولکول متانول
۳.۱ فرمول شیمیایی:
فرمول شیمیایی متانول CH3OH است که نشان دهنده یک اتم کربن، چهار اتم هیدروژن و یک اتم اکسیژن در ساختار آن است.
۳.۲ فرمول ساختاری:
فرمول ساختاری متانول آرایش اتم ها و پیوندها را نشان می دهد. این شامل یک اتم کربن است که به سه اتم هیدروژن و یک گروه هیدروکسیل (-OH) پیوند دارد.
۳.۳ گروه های عملکردی:
گروه عاملی اولیه در متانول، گروه هیدروکسیل (-OH) است که خواص شیمیایی مشخصه آن را ایجاد می کند. این گروه عاملی متانول را قادر میسازد تا در واکنشهای مختلف از جمله الکلیز، استری شدن و اکسیداسیون شرکت کند.
۳.۴ هندسه مولکولی:
متانول دارای یک هندسه مولکولی چهار وجهی است که اتم کربن در مرکز و اتم های هیدروژن و اکسیژن به آن پیوند دارند. زاویه پیوند بین اتم های کربن، اکسیژن و هیدروژن تقریباً ۱۰۹.۵ درجه است.
۳.۵ ایزومرها:
متانول به دلیل ساختار شیمیایی ساده ایزومرهای ساختاری ندارد.
۴. خواص فیزیکی:
| ویژگی فیزیکی | مقدار |
| شکل ظاهری | مایع بی رنگ با بوی ملایم و کمی شیرین |
| حالت | مایع |
| بو | متمایز و مشابه اتانول، اما کمی شیرینتر |
| طعم | سمی و تلخ، هرگز بلعیده نشود |
| نقطه ذوب | -۹۷.۶ درجه سانتیگراد |
| نقطه جوش | ۶۴.۷ درجه سانتیگراد |
| چگالی | ۰.۷۹۱۸ g/cm³ |
| حلالیت | محلول در آب و حلالهای آلی |
| ویسکوزیته | پایین |
| ضریب شکست نور | تقریباً ۱.۳۳ |
| ظرفیت گرمایی ویژه | بالا |
۵. خواص شیمیایی:
۵.۱ واکنش پذیری:
متانول واکنش پذیری متوسطی دارد و می تواند تحت واکنش های شیمیایی مختلفی قرار گیرد. می تواند در الکلیز، استری شدن، اکسیداسیون و سایر واکنش ها شرکت کند.
۵.۲ پایداری:
در شرایط عادی، متانول پایدار است. با این حال، می تواند در حضور گرما یا کاتالیزورهای خاص تجزیه شود و مونوکسید کربن و گاز هیدروژن را تشکیل دهد.
۵.۳ قابلیت احتراق:
متانول بسیار قابل اشتعال است و می تواند در حضور منبع اشتعال مانند شعله باز یا جرقه مشتعل شود. هنگام نگهداری و نگهداری متانول باید بسیار احتیاط کرد.
۵.۴ خواص اسید-باز:
متانول به عنوان یک اسید ضعیف عمل می کند و یک پروتون را به بازهای قوی می دهد. می تواند با بازهای قوی واکنش داده و نمک های آلکوکسید را تشکیل دهد.
۵.۵ واکنشهای ردوکس:
متانول میتواند تحت واکنشهای اکسیداسیون، جایی که الکترون اهدا میکند، و واکنشهای کاهشی، جایی که الکترونها را میپذیرد، انجام شود. این واکنش های ردوکس، متانول را به یک معرف مفید در تبدیل های شیمیایی مختلف تبدیل می کند.
۵.۶ هیدرولیز:
متانول به راحتی تحت شرایط عادی هیدرولیز نمی شود. با این حال، می تواند با آب در حضور یک کاتالیزور واکنش داده و فرمالدئید را تشکیل دهد.
۵.۷ خورندگی:
متانول برای اکثر مواد معمولی خورنده نیست. با این حال، می تواند فلزات و ترکیبات لاستیکی خاصی را در طول زمان خورده کند.
۵.۸ پلیمریزاسیون:
متانول در شرایط عادی پلیمریزه نمی شود.
۵.۹ سایر واکنش های شیمیایی:
• متانول می تواند با اسیدهای کربوکسیلیک واکنش داده و از طریق واکنش های استریفیکاسیون، استرها را تشکیل دهد.
• می توان آن را به فرمالدئید یا بیشتر به اسید فرمیک اکسید کرد.
• متانول می تواند دچار کم آبی شود و دی متیل اتر را تشکیل دهد.
۶. کاربردها:
۶.۱ برجسته کردن کاربردهای مختلف:
متانول کاربردهای گسترده ای در صنایعی مانند:
• ساخت مواد شیمیایی: متانول به عنوان ماده خام برای تولید فرمالدئید، اسید استیک و سایر مواد شیمیایی عمل می کند.
• بخش انرژی: متانول به عنوان سوخت در موتورهای احتراق داخلی، پیل های سوختی و به عنوان یک جزء ترکیبی در بنزین استفاده می شود.
• حلال و معرف: متانول به عنوان یک حلال و معرف همه کاره در آزمایشگاه ها و صنایع عمل می کند.
• پلاستیک و الیاف: متانول در تولید پلاستیک، رزین، الیاف مصنوعی و پوشش ها استفاده می شود.
• داروها: متانول در سنتز ترکیبات دارویی مختلف نقش دارد.
• ضد یخ: متانول جزء ترکیبات ضد یخ است.
۶.۲ خواص و کاربردها:
خواصی که متانول را برای این کاربردها مناسب می کند عبارتند از سمیت کم، اشتعال پذیری بالا، خواص حلال خوب و توانایی آن برای شرکت در انواع واکنش های شیمیایی.
۶.۳ نمونههایی از محصولات یا فرآیندها:
نمونههایی از محصولات یا فرآیندهای شامل متانول عبارتند از:
• تولید فرمالدئید برای ساخت رزین و پلاستیک.
• وسایل نقلیه متانول یا پیل سوختی برای تولید انرژی پاک.
• استفاده از متانول به عنوان حلال در فرمولاسیون های دارویی.
• ترکیب متانول به عنوان یک عامل ضد یخ در سیستم های خنک کننده خودرو.
۷. روش تولید:
۷.۱ مواد خام:
تولید متانول معمولاً به مونوکسید کربن، گاز هیدروژن و یک کاتالیزور مانند کاتالیزورهای مبتنی بر مس یا زئولیت نیاز دارد.
۷.۲ روش های تولید:
روش های متعددی برای تولید متانول وجود دارد، از جمله:
• رفرمینگ گاز طبیعی با بخار: متانول را می توان با رفرمینگ بخار کاتالیزوری گاز طبیعی تولید کرد که در آن متان با بخار واکنش می دهد و گاز سنتز (مخلوطی از هیدروژن و مونوکسید کربن) تولید می کند. سپس گاز سنتز از طریق واکنش سنتز متانول به متانول تبدیل می شود.
• تبدیل به گاز زغال سنگ: زغال سنگ را می توان برای تولید گاز سنتز گازی کرد و سپس به متانول تبدیل می شود.
• تبدیل زیست توده: زیست توده، مانند ضایعات چوب یا کشاورزی، می تواند از طریق فرآیندهای گازسازی یا پیرولیز به گاز سنتز تبدیل شود. گاز سنتز متعاقباً به متانول تبدیل می شود.
• هیدروژناسیون دی اکسید کربن: دی اکسید کربن و گاز هیدروژن می توانند در حضور یک کاتالیزور با یکدیگر واکنش داده و متانول تولید کنند. این فرآیند با استفاده از آن به عنوان ماده اولیه به کاهش انتشار دی اکسید کربن کمک می کند.
۷.۳ مراحل فرآیند:
تولید متانول شامل چندین مرحله کلیدی است:
• تهیه گاز سنتز: مواد خام، مانند گاز طبیعی یا زغال سنگ، برای تولید گاز سنتز حاوی هیدروژن و مونوکسید کربن، تحت یک فرآیند تبدیل به گاز یا اصلاح می شوند.
• سنتز متانول: گاز سنتز سپس تحت واکنش سنتز متانول قرار می گیرد که معمولاً در دماها و فشارهای بالا رخ می دهد. کاتالیزورها، مانند کاتالیزورهای مبتنی بر مس، برای تسهیل واکنش و ترویج تشکیل متانول استفاده می شوند.
• جداسازی و خالص سازی: محصول متانولی از طریق فرآیندهای تقطیر و خالص سازی از گازها، ناخالصی ها و محصولات جانبی واکنش نداده جدا می شود. این امر تولید متانول با خلوص بالا را تضمین می کند.
• بازیافت و بهینه سازی: مقداری از گاز سنتز واکنش نداده به فرآیند بازیافت می شود تا کارایی و عملکرد را بهبود بخشد. استراتژیهای بهینهسازی مختلف، مانند تنظیم دما، فشار و ترکیب کاتالیزور، برای افزایش تولید متانول استفاده میشوند.
۷.۴ کاتالیز:
کاتالیزورها نقش مهمی در فرآیند تولید متانول دارند. کاتالیزورهای مبتنی بر مس، مانند کاتالیزورهای اکسید روی مس، اکسید آلومینیوم، معمولا استفاده می شوند. این کاتالیزورها سرعت واکنش و گزینش پذیری را افزایش می دهند و تبدیل موثر گاز سنتز به متانول را ممکن می سازند.
۷.۵ شرایط واکنش:
شرایط واکنش بهینه برای سنتز متانول به کاتالیزور و فرآیند خاص مورد استفاده بستگی دارد. به طور معمول، واکنش در دمای حدود ۲۰۰-۳۰۰ درجه سانتیگراد (۳۹۲-۵۷۲ درجه فارنهایت) و فشارهای تقریباً ۵۰-۱۰۰ اتمسفر انجام می شود. شرایط دقیق ممکن است بسته به فعالیت کاتالیزور و بازده متانول مورد نظر متفاوت باشد.
۷.۶ مقیاس تولید:
تولید متانول می تواند در مقیاس های مختلف، از تولید آزمایشگاهی در مقیاس کوچک تا تأسیسات صنعتی در مقیاس بزرگ، رخ دهد. کارخانههای متانول در مقیاس صنعتی ظرفیتهای تولید بالایی برای برآورده کردن نیازهای کاربردهای مختلف دارند.
۷.۷ مصرف انرژی و کارایی:
تولید متانول به دلیل نیاز به دما و فشار بالا، فرآیندی انرژی بر است. با این حال، پیشرفت در فناوری فرآیند و استفاده از گرمای اتلاف یا منابع انرژی تجدید پذیر می تواند به بهبود بهره وری انرژی کمک کند. استراتژی های مختلف بازیافت انرژی و بهینه سازی برای به حداقل رساندن مصرف انرژی و افزایش کارایی کلی فرآیند به کار گرفته شده است.
۷.۸ اثرات زیست محیطی:
تولید متانول به دلیل اتکا به سوخت های فسیلی یا مواد اولیه زیست توده می تواند پیامدهای زیست محیطی داشته باشد. انتشار دی اکسید کربن ممکن است با فرآیند تولید مرتبط باشد، به خصوص هنگام استفاده از فسیلسوخت ها با این حال، استفاده از دی اکسید کربن به عنوان ماده اولیه می تواند به کاهش این انتشار کمک کند. علاوه بر این، تلاش برای بهبود بهره وری انرژی و استفاده از منابع تجدیدپذیر می تواند ردپای کلی محیطی تولید متانول را کاهش دهد.
۷.۹ نوآوری ها و پیشرفت های فرآیند:
نوآوری های اخیر در تولید متانول بر بهبود کارایی انرژی، کاهش انتشار کربن و استفاده از مواد اولیه جایگزین تمرکز دارد. کاتالیزورهای پیشرفته، تنظیمات فرآیند جایگزین و ادغام منابع انرژی تجدیدپذیر به تولید متانول پایدارتر و مقرون به صرفه تر کمک می کند.
۷.۱۰ تحولات آتی:
تحقیق و توسعه مداوم در تولید متانول با هدف افزایش بیشتر کارایی فرآیند، کاهش اثرات زیست محیطی و کشف مواد اولیه جایگزین. پیشرفتها در طراحی کاتالیزور، مهندسی راکتور و یکپارچهسازی فرآیند ممکن است راه را برای تولید متانول پایدارتر و اقتصادیتر در آینده هموار کند.
۸. اثرات زیست محیطی:
۸.۱ تجزیه پذیری زیستی:
متانول به راحتی در محیط زیست تخریب پذیر است. میکروارگانیسم ها می توانند متانول را متابولیزه کرده و آن را به ترکیبات ساده تری تجزیه کنند.
۸.۲ پایداری:
متانول در محیط پایدار نیست و از طریق تجزیه زیستی یا تبخیر نسبتاً سریع تجزیه می شود.
۸.۳ سمیت:
متانول زمانی که خورده، استنشاق یا از طریق پوست جذب می شود برای انسان و حیوانات سمی است. این می تواند اثرات شدید سلامتی، از جمله اختلال بینایی، آسیب به سیستم عصبی مرکزی و حتی مرگ ایجاد کند.
۸.۴ مقررات زیست محیطی:
مقررات و دستورالعمل های مختلفی برای اطمینان از حمل، ذخیره سازی و دفع ایمن متانول وجود دارد. هدف این مقررات حفاظت از سلامت انسان و محیط زیست در برابر خطرات احتمالی مرتبط با استفاده از متانول است.
۸.۵ نگرانی های زیست محیطی:
نگرانی های زیست محیطی مربوط به متانول شامل احتمال آلودگی آب و خاک در صورت نشت یا دفع نادرست است. اثرات سمی متانول بر زندگی آبزیان و پتانسیل تجمع زیستی در زنجیره غذایی نیز از موارد نگران کننده است.
۸.۶ کاهش و بهترین شیوه ها:
بهترین شیوه ها برای کاهش اثرات زیست محیطی متانول شامل روش های نگهداری، نگهداری و دفع مناسب است. اجرای اقدامات مهار، استفاده از تجهیزات حفاظتی مناسب و رعایت مقررات برای به حداقل رساندن خطرات زیست محیطی حیاتی است.
۸.۷ تحقیق و توسعه:
تحقیقات در حال انجام بر درک سرنوشت و رفتار متانول در محیط زیست، ارزیابی خطرات بالقوه، و توسعه راه حل های پایدار متمرکز است. همچنین تلاشها به سمت توسعه جایگزینهای سبزتر و روشهای تولید سازگار با محیط زیست انجام میشود.
۸.۸ ابتکارات پایداری:
هدف ابتکارات پایداری ترویج استفاده مسئولانه و مدیریت متانول است. این ابتکارات شامل توسعه فرآیندهای تولید متانول سبز و تجدیدپذیر و همچنین ایجاد برنامه های صدور گواهینامه و برچسب های زیست محیطی است.
۹. نتیجه گیری:
در نتیجه متانول یک ترکیب شیمیایی قابل توجه با کاربردهای متنوع در صنایع است. خواص منحصر به فرد و طیف وسیع کاربرد آن، آن را به یک جزء ضروری در محصولات و فرآیندهای مختلف تبدیل کرده است. با این حال، مدیریت، استفاده و دفع مسئولانه متانول برای کاهش خطرات بالقوه زیست محیطی و بهداشتی آن بسیار مهم است. همانطور که به جلو می رویم، پیشرفت های بیشتر در روش های تولید متانول، اقدامات ایمنی و پایداری زیست محیطی به اهمیت مداوم و تأثیر مثبت آن کمک خواهد کرد.
۹.۱ اهمیت:
اهمیت متانول در نقش آن به عنوان یک ترکیب شیمیایی همه کاره است که به نوآوری کمک می کند، فرآیندهای صنعتی را هدایت می کند و به پیشرفت در تولید و ذخیره انرژی کمک می کند. کاربردهای آن در سراسر صنایع، آن را به بخشی جدایی ناپذیر از جامعه مدرن ما تبدیل کرده است.
۹.۲ تأثیر:
متانول تأثیر قابل توجهی بر جنبه های مختلف زندگی ما دارد، از نیرو دادن به وسایل نقلیه و تولید انرژی پاک گرفته تا تولید مواد ضروری و داروها. با این حال، مهم است که پیامدهای منفی بالقوه مرتبط با سمیت و اثرات زیست محیطی آن را بشناسیم و به آنها رسیدگی کنیم.
۹.۳ چشم انداز آینده:
آینده متانول دارای تحولات امیدوارکننده ای از نظر بهبود بازده تولید، فرآیندهای سبزتر و استفاده پایدار از مواد اولیه است. تحقیقات در حال انجام و پیشرفت های تکنولوژیکی به شکل دادن به آینده متانول ادامه خواهد داد و راه را برای کاربردهای ایمن تر و سازگار با محیط زیست هموار می کند.
۹.۴ بیانیه پایانی جذاب:
همانطور که ما پتانسیل کامل متانول را باز می کنیم و احتمالات آینده آن را بررسی می کنیم، اجازه دهید مسئولیت خود را برای رسیدگی به این ترکیب شیمیایی با احتیاط حفظ کنیم. با پذیرش شیوههای پایدار و ترویج نوآوری، میتوانیم از قدرت متانول استفاده کنیم و در عین حال تأثیر آن را بر سلامت انسان و محیط زیست به حداقل برسانیم.





نظرات